 Sel elektrolisis, yaitu sel yang mengubah energi listrik
menjadi energi kimia. Arus listrik digunakan untuk melangsungkan reaksi redoks tak
spontan. Pada sel elektrolisis, reaksi kimia akan terjadi jika arus
listrik dialirkan melalui larutan elektrolit. Sel elektrolisis memiliki 3 ciri utama, yaitu :
Sel elektrolisis, yaitu sel yang mengubah energi listrik
menjadi energi kimia. Arus listrik digunakan untuk melangsungkan reaksi redoks tak
spontan. Pada sel elektrolisis, reaksi kimia akan terjadi jika arus
listrik dialirkan melalui larutan elektrolit. Sel elektrolisis memiliki 3 ciri utama, yaitu : - Ada larutan elektrolit yang mengandung ion bebas.
- Ada 2 elektroda dalam sel elektrolisis.
- Ada sumber arus listrik dari luar, seperti baterai yang mengalirkan arus listrik searah (DC).
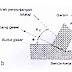
SUSUNAN
SEL ELEKTROLISIS
ATURAN SEL ELEKTROLISIS
1) Kation yang
sukar tereduksi pada katoda sel
elektrolisis, yaitu logam alkali (IA),
logam alkali tanah (IIA), Al dan Mn.
2)
Elektroda
inert adalah elektroda yang sukar bereaksi, yaitu elektroda Pt, Au dan C.
REAKSI-REAKSI SEL
ELEKTROLISIS - KATODA
- Jika kation sukar tereduksi, maka H2O tereduksi menjadi H2
2. Jika kation tidak sukar tereduksi, maka
kation logam tersebut yang tereduksi menjadi logamnya
3. Ion H+ dari asam tereduksi menjadi H2

4. Jika
elektrolit berupa lelehan/leburan
(tidak mengandung air), maka kation apapun
tetap tereduksi menjadi logamnya.

REAKSI-REAKSI SEL
ELEKTROLISIS – ANODA
Jika elektroda tidak inert, maka yang teroksidasi
adalah anoda
Jika elektroda inert maka,
1.
Ion OH- dari basa teroksidasi
menjadi O2
2 .
Ion halida teroksidasi menjadi gas
halogen
3.
Jika ion sisa asam yang mengandung
O atau F, maka air teroksidasi menjadi O2
HUKUM-HUKUM FARADAY
• Hukum-hukum Faraday menjelaskan tentang hukum kelistrikan yang
berkaitan dengan sel elektrolisis
• Hukum Faraday I : Massa zat yang
dihasilkan (G) berbanding lurus dengan arus listrik yang melalui elektrolisis
• Hukum Faraday II : Massa zat yang
dihasilkan (G) pada elektrolisis sebanding dengan massa ekuivalen zat (ME)
tersebut.

























A true vintage-tinted design with a titanium frame
BalasHapusAn authentic classic design 개집 왕 with a traditional 벳 인포 steel frame. The titanium pot classic titanium price per ounce design micro touch titanium trimmer with a standard design and an attractive chrome finish.